|
KOVALENT BAĞ
Ametal atomları kararlı yapıya ulaşmak için son yörüngedeki bazı elektronlarını ortaklaşa kullanırlar. Atomlar arasında elektronların ortaklaşa kullanılmasıyla oluşan bağa kovalent bağ denir. Örneğin iki hidrojen atomu elektronlarını ortaklaşa kullanarak aralarında kovalent bağ oluşturur. Böylece her bir hidrojen atomu kararlı hale gelir.
Hidrojen gibi birçok ametal başka ametallerle bileşik oluştururlar. CO, H2O, NO2, CO2 bunlardan bazılarıdır.
Kovalent bağ Ametal atomları arasında yani Anyonlar ( - iyonlar) arasında olur. Sulu çözeltileri elektrik akımızı iletmezler. Önemli Ametal atomlar ( İyot=I , karbon=C , fosfor = P , kükürt = S katı ) ( Brom= Br sıvı ) ( Azot=N , Oksijen=O, Hidrojen=H klor=Cl gaz ) dır.
Molekül
Kovalent bağlı bileşiklerin en küçük birimi moleküldür. Moleküller maddenin tüm özelliklerini gösterir ve bağımsız olarak hareket edebilir. Aynı cins atomlardan oluşan moleküller element molekülleridir. O2, H2, F2, N2 element molekülleridir. Bunlar bileşik değildir. Farklı cins atomların molekülleri bileşik moleküllerini oluşturur. H2O, CO2, NH3 bileşik molekülleridir.
X2 2 adet X atomu kovalent bağ yaparak X2 molekülünü oluşturmuştur.
Y3 3 adet Y atomu kovalent bağ yaparak Y3 molekülünü oluşturmuştur.
Oksijen (O2) molekülünün bağ yapısı
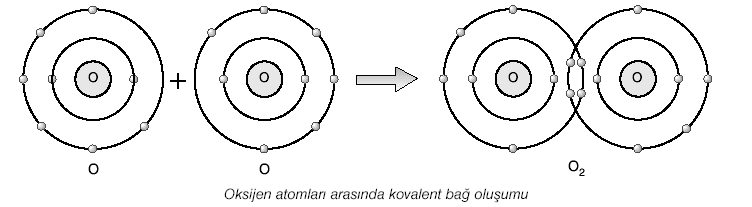
Oksijenin son yörüngesinde 6 elektron vardır. Bir oksijen atomu son yörüngesindeki 2 elektronunu başka bir oksijen atomunun son yörüngesindeki 2 elektron ile ortaklaşa kullanır. Böylece her bir oksijen atomunun elektron dizilişi kararlı olur. Oksijen atomlarının kovalent bağ yapması sonucunda her birinin çevresinde 10 e– dolanır.
Su molekülünün bağ yapısı Bir su molekülü 2 H ve bir O atomunun kovalent bağ yapması sonucu oluşur. H atomlarından her biri kendi e- unu O atomunun bir
elektronu ile ortaklaşa kullanır.
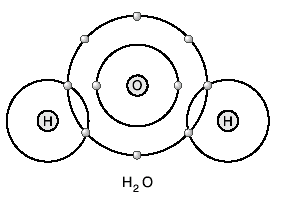
Böylece hem H, hem de O atomları kararlı hale gelir.
Bir su molekülü 2 hidrojen ve 1 oksijen atomundan
oluştuğu için, su molekülü H2O şeklinde yazılır.
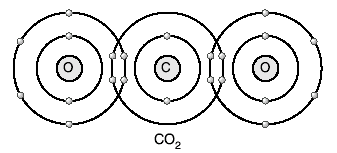
Karbon dioksit molekülünün bağ yapısı
Karbonun elektron dizilişi 6 C ) ) şeklindedir.
2 4
  
|
|
Bu konu 114611 kez okundu |
|
Bu konuyu Site Admini Ekledi |